
用于YY0506-2009《病人、医护人员和器械用手术单、手术衣和洁净服》系列标准中的手术衣。手术衣在《医疗器械分类目录》中为第二类医疗器械产品,类代号为6864。 一次性使用手术衣的..
138-2432-8299 立即咨询 扫码咨询
扫码咨询
发布时间:2020-12-31 热度:
用于YY0506-2009《病人、医护人员和器械用手术单、手术衣和洁净服》系列标准中的手术衣。手术衣在《医疗器械分类目录》中为第二类医疗器械产品,类代号为6864。
一次性使用手术衣的结构和组成
一次性使用手术衣为手术人员穿着以防止感染原传播的长袍,由前身、后身、袖子、系带等组成。
一次性使用手术衣相关标准
GB 15980-1995 一次性使用医疗用品卫生标准
GB 18278-2000 医疗保健产品灭菌确认和常规控制要求 工业湿热灭菌
GB 18279-2000 医疗器械 环氧乙烷灭菌确认和常规控制
GB 18280-2000 医疗保健产品灭菌确认和常规控制要求 辐射灭菌
GB/T 16886.1-2001 医疗器械生物学评价 第1部分:评价与试验
GB/T 16886.7-2001 医疗器械生物学评价 第7部分:环氧乙烷灭菌残留量
GB/T 16886.10-2005 医疗器械生物学评价 第10部分:刺激与迟发型超敏反应试验
GB/T 19633-2005 最终灭菌医疗器械的包装
GB/T 14233.1-2008 医用输血、输液、注射器具检测方法 第1部分:化学分析方法
GB/T 14233.2-2008 医用输血、输液、注射器具检测方法 第2部分:生物试验方法
YY/T 0313-1998 医用高分子制品包装、标志、运输和贮存
YY/T 0287-2003 医疗器械 质量管理体系用于法规的要求
YY 0466-2003 医疗器械 用于医疗器械标签、标记和提供信息的符号
YY/T 0615.1-2007 标示“无菌”医疗器械的要求 第1部分:最终灭菌医疗器械的要求
YY/T 0316-2008 医疗器械 风险管理对医疗器械的应用
YY /T 0506.1 病人、医护人员和器械用手术单、手术衣和洁净服第1部分:制造厂、处理厂和产品的通用要求
YY /T 0506.2 病人、医护人员和器械用手术单、手术衣和洁净服第2部分:性能要求和性能水平
YY /T 0506.3 病人、医护人员和器械用手术单、手术衣和洁净服第3部分:试验方法
YY /T 0506.4 病人、医护人员和器械用手术单、手术衣和洁净服第4部分:干态落絮试验方法(ISO 9073-10:2003,IDT)
YY /T 0 506.5 病人、医护人员和器械用手术单、手术衣和洁净服第5部分:阻干态微生物穿透试验方法
YY /T 0506.6 病人、医护人员和器械用手术单、手术衣和洁净服第6部分:阻湿态微生物穿透试验方法
中华人民共和国药典
一次性使用手术衣的主要危害
危害类型 | 可能产生的危害 | 形成因素 | 控制措施 |
生物学危害 | 生物污染 | 产品没有灭菌或灭菌没有达到标准 | 严格控制灭菌工艺 |
环境污染 | 生产环境污染产品,如包装破损、外来的纤维、粉尘、细菌、其它杂质等 | 严格控制生产环境及包装工艺 | |
生物相容性 | 生产引入了外来有害物质没有被有效去除;环氧乙烷残留量超标 | 原材料入厂检验; 严格控制灭菌工艺 | |
与产品使用相关的危害 | 不适当的标签 | 外部标记不全面、标记不正确或不能够清楚易认 | 标记印刷清晰正确;标记内容按相关要求标记全面。 |
说明书上的注意事项不全 | 如缺少详细的使用方法、缺少必要的警告说明; 使用前未检查产品灭菌或包装状态; 产品等级标示不清 | 规范说明书; 说明书上提示 | |
由不熟练或未经训练的人员使用 | 使用者未经培训或培训不足,不能正确使用产品; | 使用前培训 | |
对一次性使用产品的很可能再次使用的危害性警告不适当 | 说明书中未包含只限一次性使用 | 规范说明书 | |
功能失效引起的危害 | 不适当的预期用途表述 | 说明书中未能清楚表明产品用途 | 规范说明书 |
不适当的产品包装 | 生产、运输、搬运和储存过程中导致包装破损; 包装封口不严密; 包装材料选择不适当 | 规范包装 | |
失去产品的完整性 | 产品各构件之间缝制或粘合达不到隔离要求; | 严格控制生产工艺、产品检验 |
一次性使用手术衣主要技术指标
1.规格尺寸和允差要求。
2.YY/T0506-2009《病人、医护人员和器械用手术单、手术衣和洁净服》中性能要求见下表:
性能名称 | 单位 | 要求 | |||
标准性能 | 高性能 | ||||
产品关键区域 | 产品非关键区域 | 产品关键区域 | 产品非关键区域 | ||
阻微生物穿透,干态 | Log10 CFU | 不要求 | ≤2a,c | 不要求 | ≤2a,c |
阻微生物穿透,湿态 | IB | ≥2.8b | 不要求 | 6.0b,d | 不要求 |
洁净度,微生物 | Log10(cfu/dm2) | ≤2c | ≤2c | ≤2c | ≤2c |
洁净度,微粒物质 | IPM | ≤3.5 | ≤3.5 | ≤3.5 | ≤3.5 |
落絮 | Log10(落絮计数) | ≤4.0 | ≤4.0 | ≤4.0 | ≤4.0 |
抗渗水性 | cmH2O | ≥20 | ≥10 | ≥100 | ≥10 |
胀破强度,干态 | kPa | ≥40 | ≥40 | ≥40 | ≥40 |
胀破强度,湿态 | kPa | ≥40 | 不要求 | ≥40 | 不要求 |
拉伸强度,干态 | N | ≥20 | ≥20 | ≥20 | ≥20 |
拉伸强度,湿态 | N | ≥20 | 不要求 | ≥20 | 不要求 |
注:a试验条件:挑战菌浓度为108CFU/g滑石粉,振动时间为30min。
b用YY/T0506.6试验时,在95%的置信水平处的IB的最小显著性差异为0.98。这是区分两个材料之间有所不同的最小差异。小于等于0.98IB的材料变动可能无差异;而大于0.98IB则可能有差异(95%的置信水平意味着进行20次试验,至少有19次是正确的)。
c在本部分中log10(CFU≤2)意味着最大300CFU。
d本部分中IB=6.0时,意味着无穿透。IB=6.0是最大可接受值。
3、粘合或缝制要求
4、无菌要求
一次性使用手术衣应无菌供应,应经过一个确认过的灭菌过程使其无菌。
5、化学性能要求
一次性使用手术衣若采用环氧乙烷灭菌,环氧乙烷残留量应不大于10 mg/kg。
6、生物性能要求
一次性使用手术衣对皮肤应无刺激与迟发型超敏反应。
7、结构要求
如有系带应规定系带长度、系带固定的牢固度等。
8、透气性
如您有相关产品需要咨询,欢迎您直接来电13824328299咨询我司工作人员,获得详细的费用报价与周期等信息。

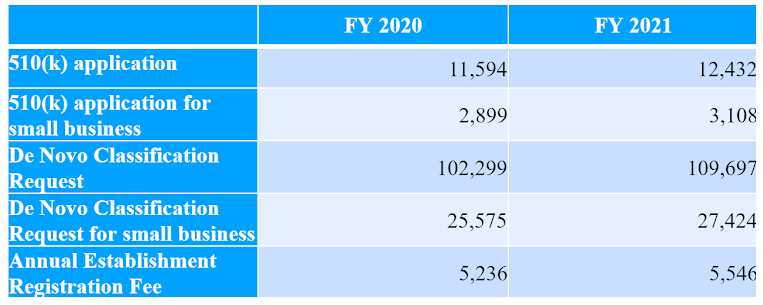
2021年医疗设备注册使用年金费用 ,2021年医疗器械FDA注册年金增至5546美金,美国食品药品监督管理局(FDA认证)已发布了针对医疗器械用户的最新费用表-申请FDA认证批准其医疗...

英国出口需要办理什么认证呢? 英国目前正处于脱欧过渡期中,该过渡期将到2020年年底为止。2020年9月1日,英国商业、能源和工业战略部在其官方网站上正式公布: 从2021年1月...

官方微信公众号
深圳市宝安82区新安六路勤业商务中心A栋一楼112-114
邮箱:yuhaoqun@ebotek.cn
微信:13824328299(同手机号码)